このページでは、がんと免疫の関係や、免疫の仕組みに注目した治療の考え方について、できるだけわかりやすくご説明しています。治療の効果や結果をお約束するものではなく、実際に治療が適しているかどうかは、検査結果や体調をふまえて医師が判断します。

目次
もうできることは尽きたと
考えておられる方へ
がん治療に限界を感じたとき、多くの方が「もう、できることは何もないのでは」と感じられています。
ですが、がんの一部には、“免疫から姿を隠す”ことで攻撃をすり抜ける性質があり、そのため手が出せず「できることは無い」という考えに陥ってしまいます。その“隠れてしまったがん”に、再び免疫の目を向けさせて再攻撃させる治療─それが「MHCクラスⅠ」という治療アプローチです。免疫の目から姿を隠したがん細胞を“見える状態”に導き、“がん”細胞を認知反応させた上で、本来の免疫力で改めて再攻撃させることを目指したものです。「治療がない」と言われた方にも、まだ選べる道、選択肢がこのように残されている、ということをこれからご説明いたします。
がんは、免疫のはたらきから見えにくくなることがあると言われています。このページでは、そうした免疫の仕組みをふまえながら、MHCクラスⅠという目印に注目した治療の考え方について、情報として整理しています。療を行うかどうかは、検査結果や病状を見ながら、医師が一人ひとり判断します。
免疫の目を欺くがん細胞
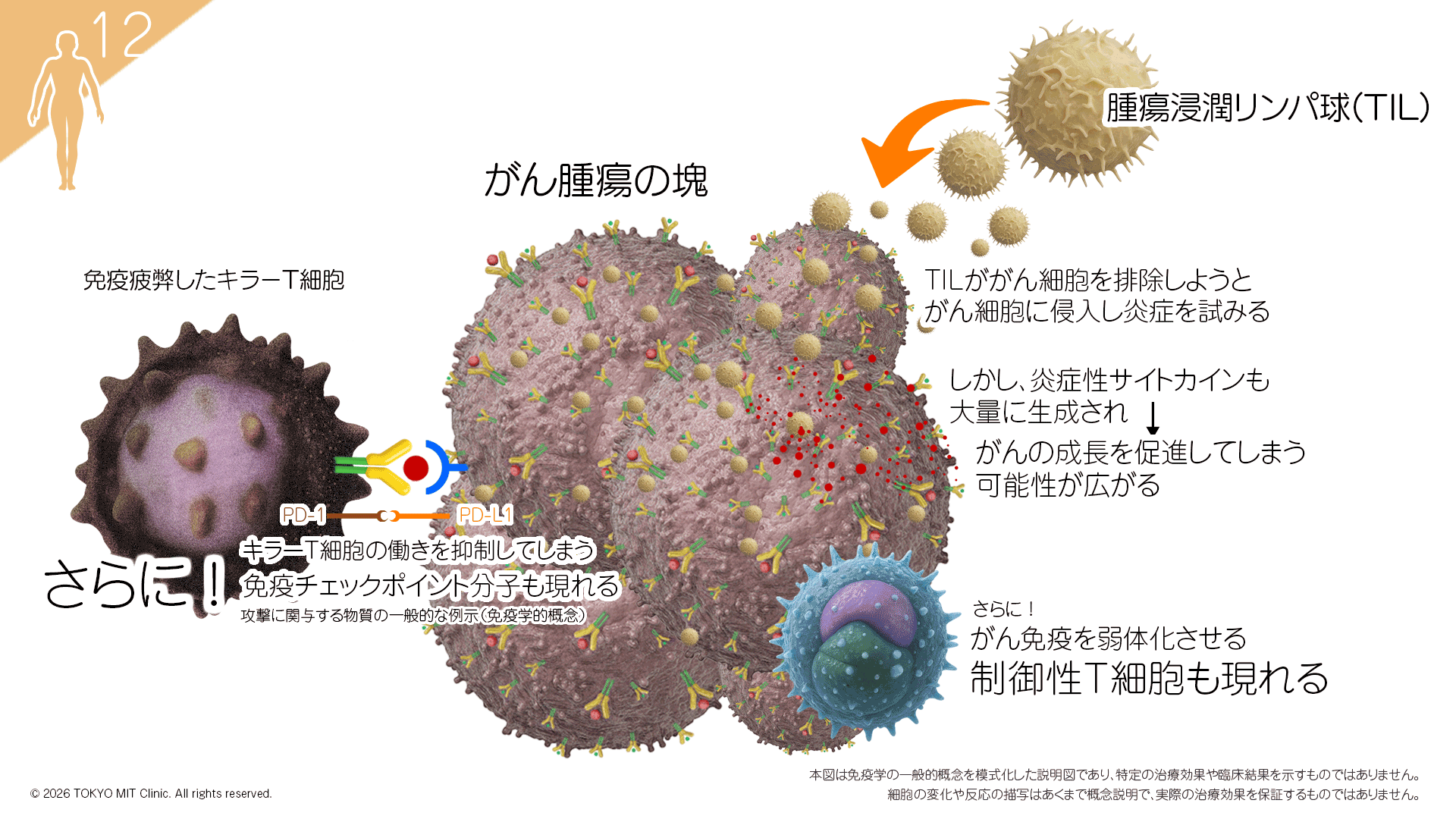
すでにご承知の通り、私たちの体には「がん細胞を見つけ出して壊す細胞=免疫」が備わっています。しかし、がん細胞は「MHCクラスⅠ」という“目印(名札)”を外すことで、免疫細胞から姿を隠してしまう性質があります。つまり、免疫が「弱く働かないのではなくがんが見えない状態」になってしまっているのです。
つまり免疫の力を強くすることに注目しすぎて、「がんを見つける方法」に注視していなかったからです。
MHCクラスⅠ誘導とは?
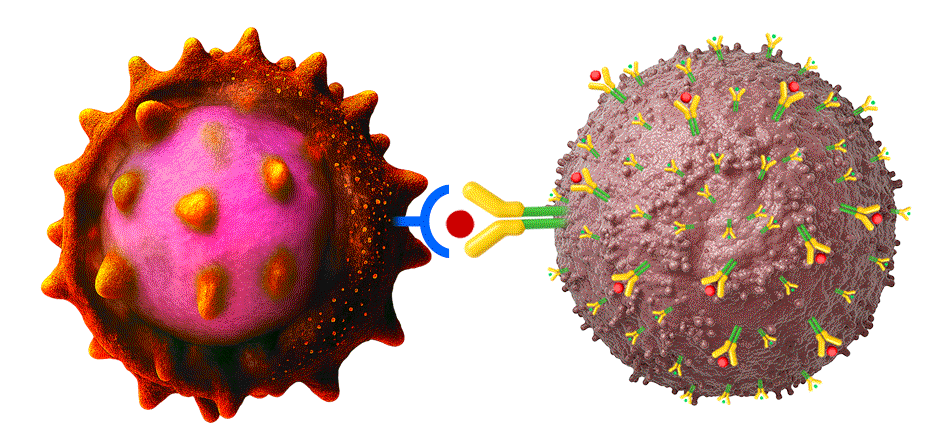
MHCクラスⅠは、免疫が細胞の状態を認識する際に関与すると考えられている分子(目印)です。
がん細胞は自らこの分子であるMHCクラスⅠを減らすことで、免疫の目から逃れようとします。
MHCクラスⅠ誘導治療キラーT細胞に認識・反応・再攻撃を促し、治療設計上の観点として検討するアプローチです。
免疫治療にはさまざまな考え方があり、治療設計の着眼点も異なります。本アプローチでは、免疫が細胞を認識する仕組み(MHCクラスI等)に着目し、検査結果や病状に応じて治療方針を検討します。
従来の免疫治療との違い

一般的な免疫治療は、免疫細胞を活性化させて攻撃力を高めるものでした。しかし、がん細胞が見えないままでは、いくら免疫を強くしても攻撃の対象を見つけることはできません。
MHCクラスⅠ誘導治療は、がん細胞を「見える化」させ、免疫が正確に標的を捉えて再攻撃できるように整え導く治療法です。
ご相談が多いケース(例)
以下は、これまでにご相談が多い状況の一例です。
治療の適応は、検査結果・病状等を踏まえて医師が個別に判断します。
■ 進行がんや再発について、今後の選択肢を知りたい方
■ これまでの治療について、別の考え方も知っておきたい方
■ 検査結果をふまえて、免疫との関係を理解したい方
■ 標準治療との併用ができるか相談したい方
■ 今後の方針を落ち着いて整理したい方

※治療の適応可否は、事前の精密検査で慎重に判断いたします。
私たちの体のなかで起こる
“がん”と免疫監視機構の戦い
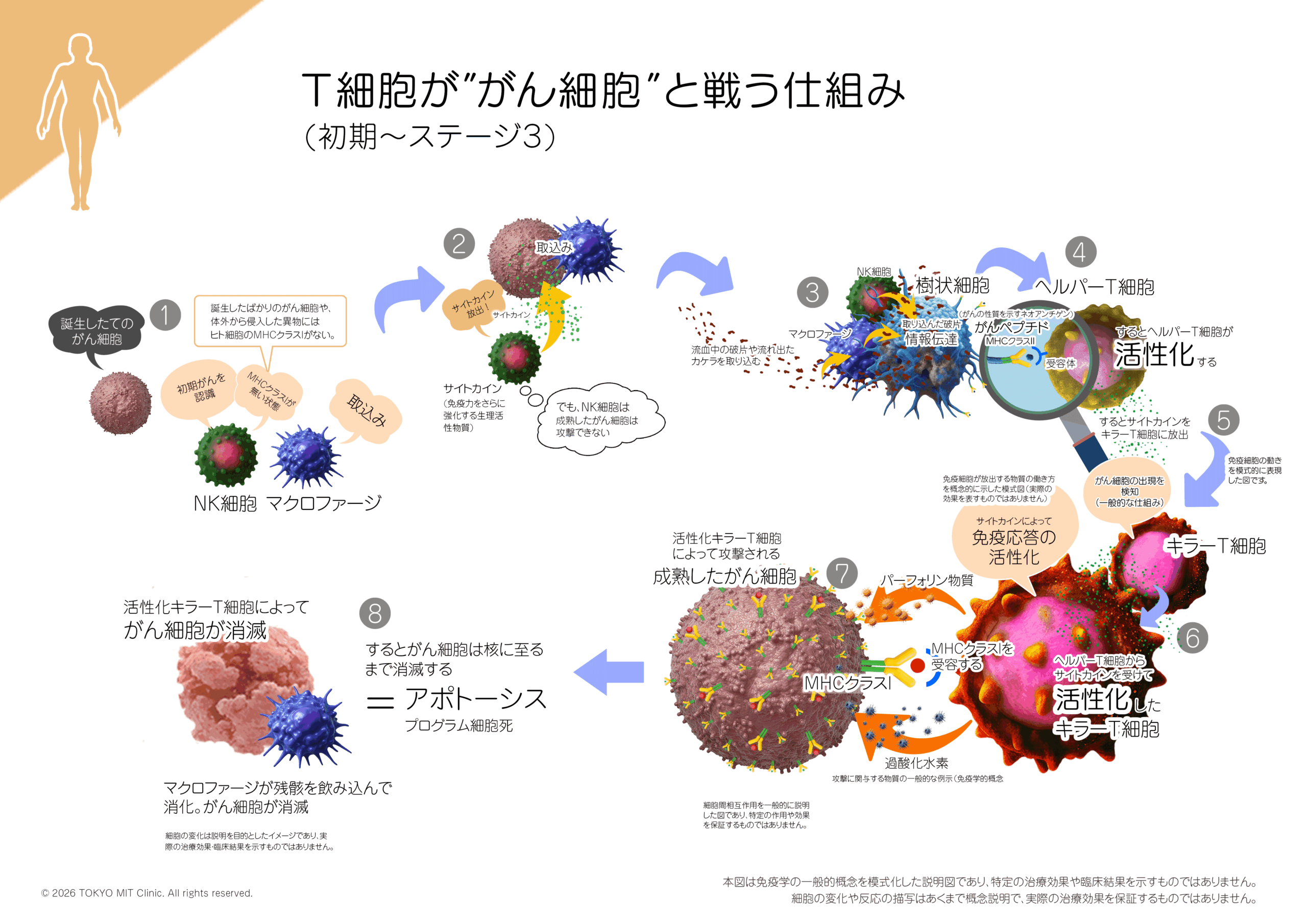
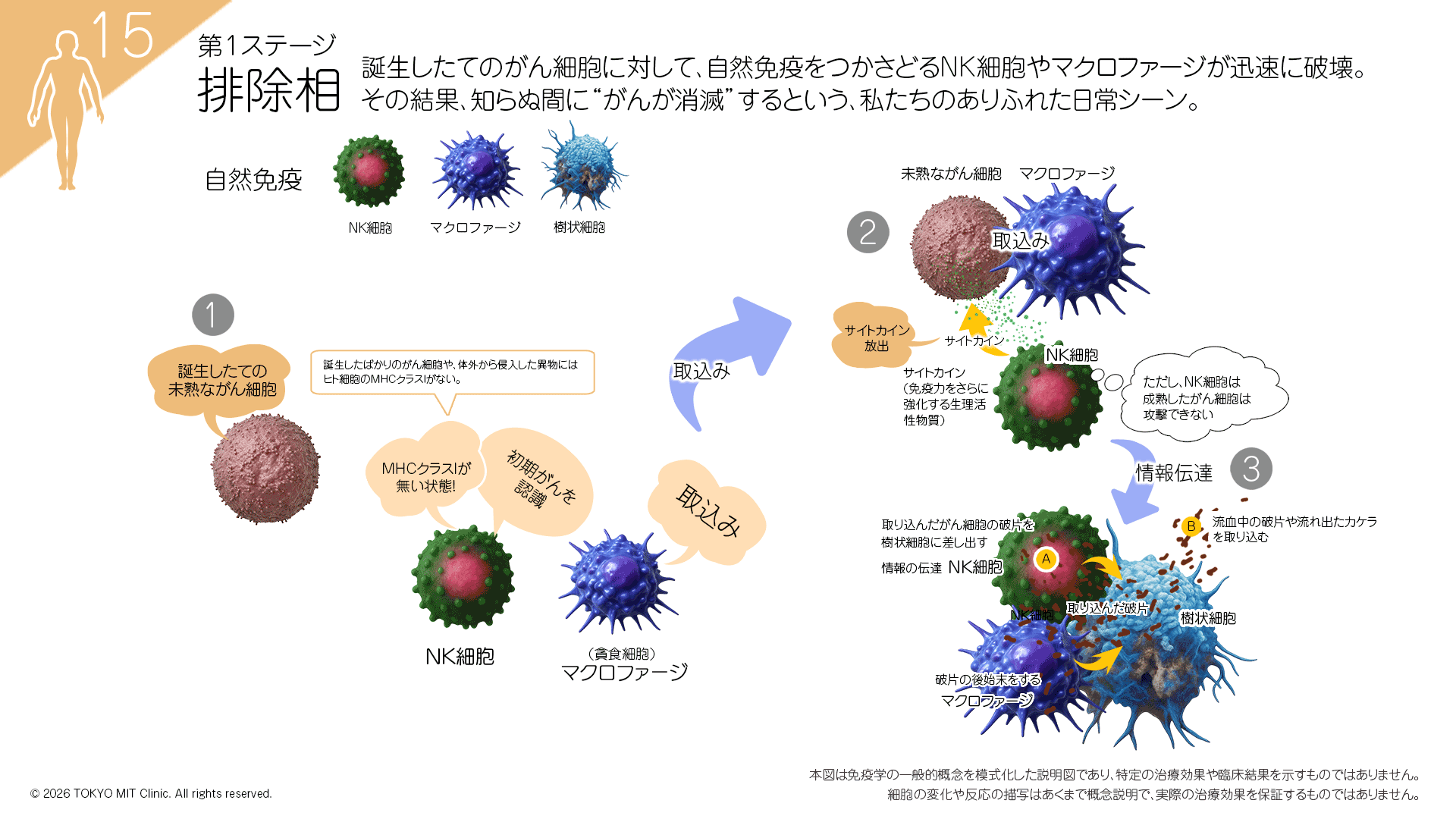
第1ラウンド:排除相(自然免疫)
出来立てのがん細胞を排除
スマホで見る → こちら
体に出現したがん細胞は、「自然免疫機構」によって、初期の段階で排除されます。多くは症状が出ないまま経過する場合もあります。
・NK細胞:異常細胞を見つけて直接攻撃
・マクロファージ/単球:異物の貪食+サイトカイン放出
・樹状細胞:がんの破片(抗原)を取り込み、T細胞に監視報告書を提示(その提示によって、獲得免疫に情報がバトンが渡される)
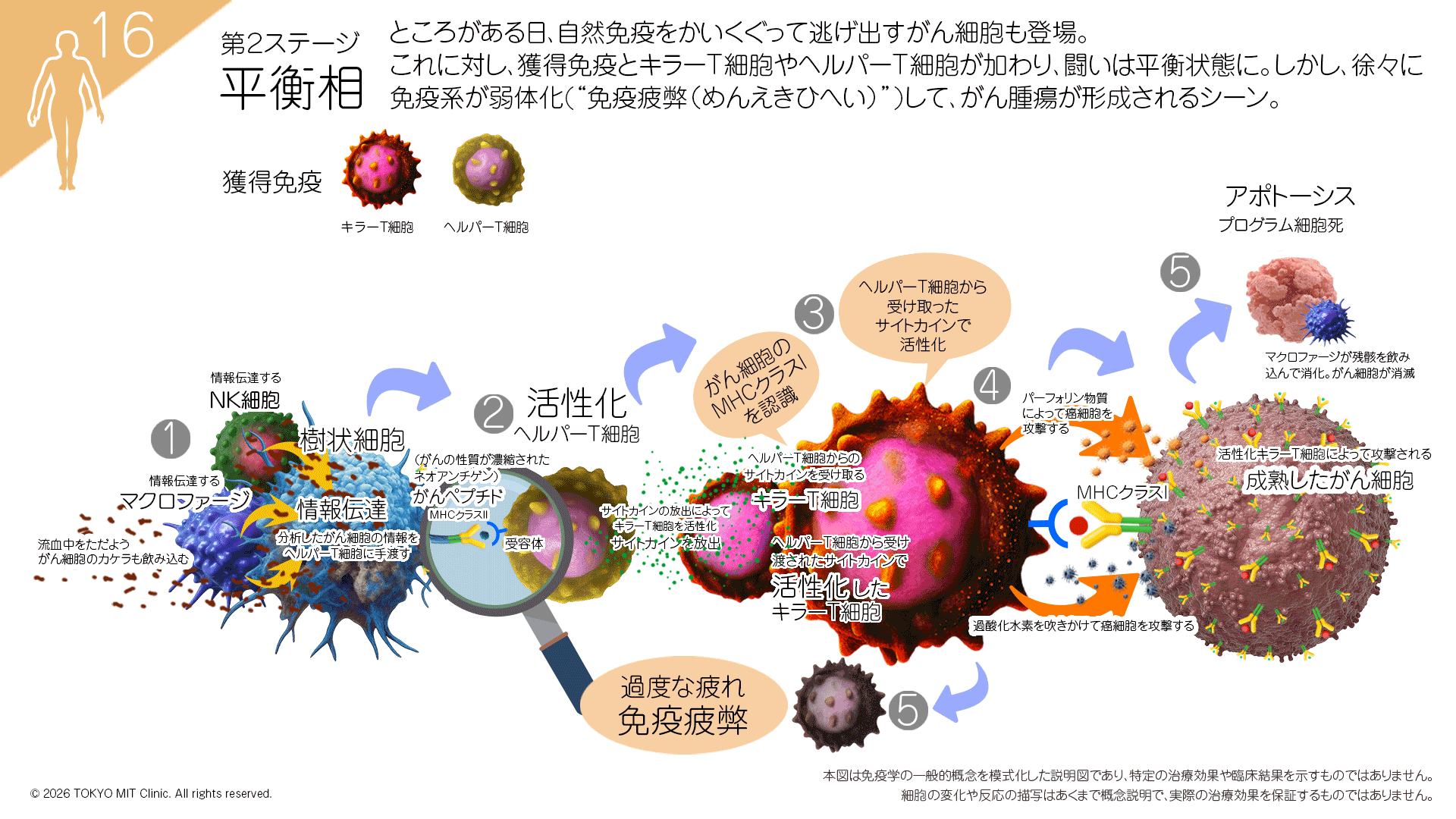
第2ラウンド:平衡相(獲得免疫)
排除を逃れたがん細胞のチーム攻撃
スマホで見る → こちら
排除がかなわないと、がん細胞は次なる「獲得免疫機構」へとバトンタッチされ、キラーT細胞による排除攻撃を受けます。しかしがん細胞はこの排除を回避しながら、生存するのに適したがん細胞へと徐々に変化する場合があります(変化することで攻撃を回避して生体内に生存可能となる訳です)。
樹状細胞:MHCクラスⅠ&Ⅱを用いて抗原提示
ヘルパーT細胞(CD4⁺):司令塔として活性化指令を出す
B細胞:抗体を準備(補助的)
キラーT細胞(CD8⁺):がん抗原を認識して「活性化」され始める(がんとの攻防が続くが、免疫逃避が始まる)
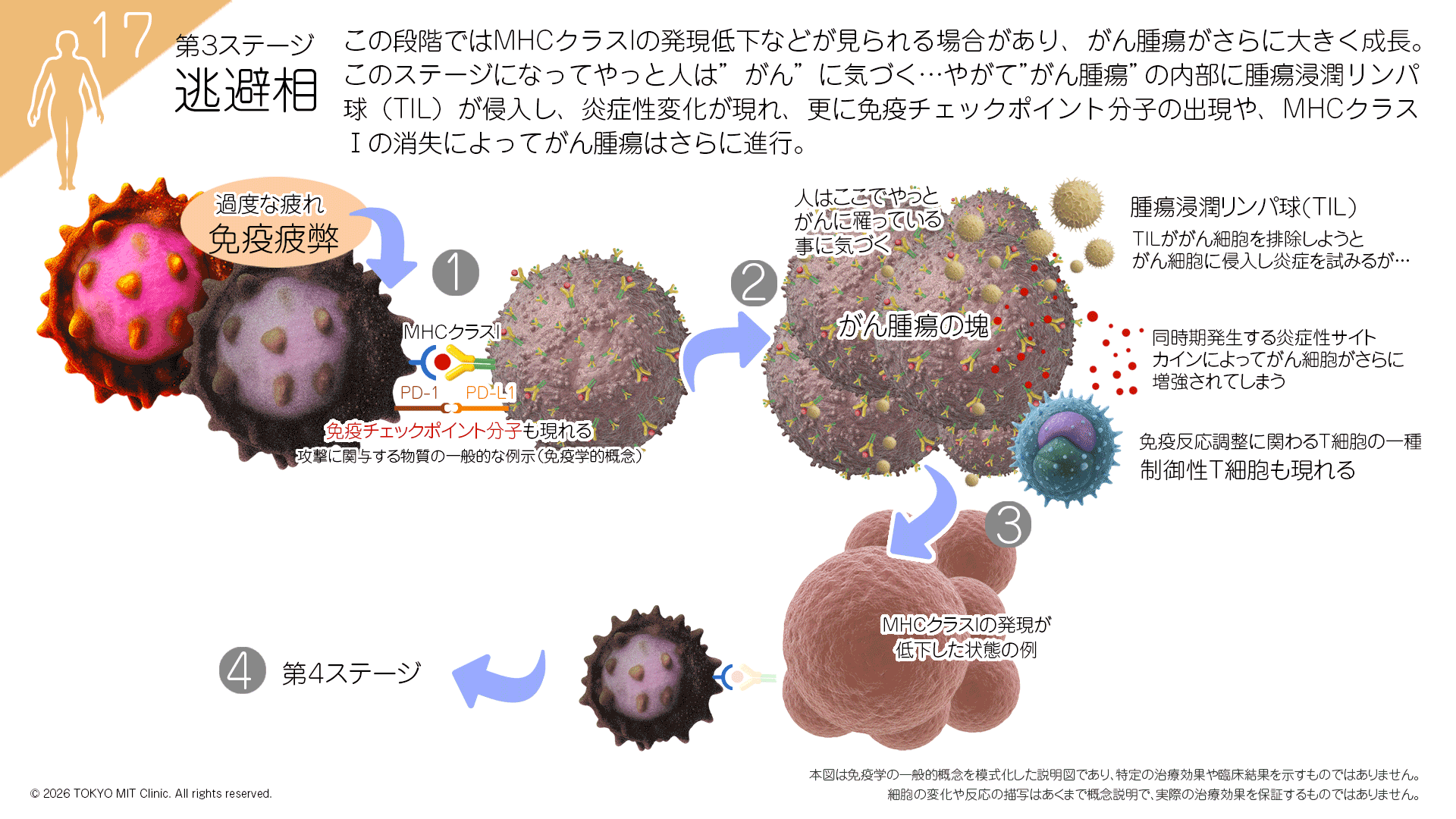
第3ラウンド:逃避相(免疫抑制)
識別マーカーを隠して逃れるがん細胞
スマホで見る → こちら
こうして長い戦いの中で、「免疫に見つからない」ように擬態化する能力「免疫抑制機構」を獲得しながら、癌細胞は免疫の攻撃をかいくぐって増殖し始める場合があります。つまり「編集」されたがん細胞の集団となります。(この状態から著しく進んだのが、進行がん・末期がん相当と呼ばれる状態です)。
がん細胞が:MHCクラスⅠを減少・消失、PD-L1などでT細胞を無力化、免疫抑制性マクロファージやTreg細胞を誘導し、その結果、免疫反応が十分に働きにくくなる場合があります。。
ここから先の第4ラウンドが、治療方針を考える際の重要な部分であり私たちが目指す姿です。
▼
第4段階:再攻撃を目指す
MHCクラス1の復活
免疫監視機構のメカニズムを復活させ、がん細胞に対し「強力な免疫応答を誘導する目印の再現」、つまり、MHCクラスⅠを復活させ、免疫細胞に再攻撃させる治療を目指しています。
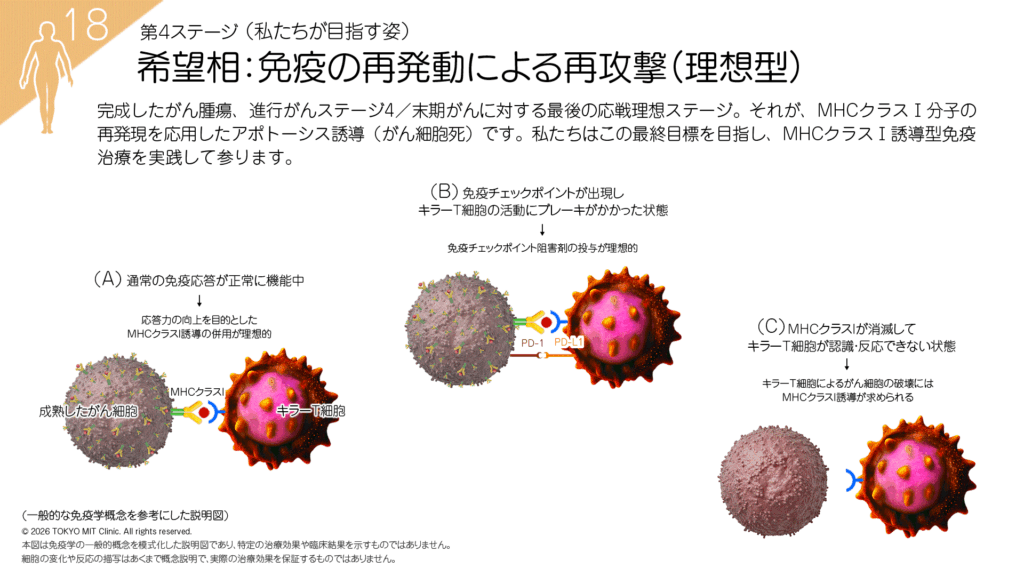
MHCクラスⅠ誘導型治療
過去の治療がん腫
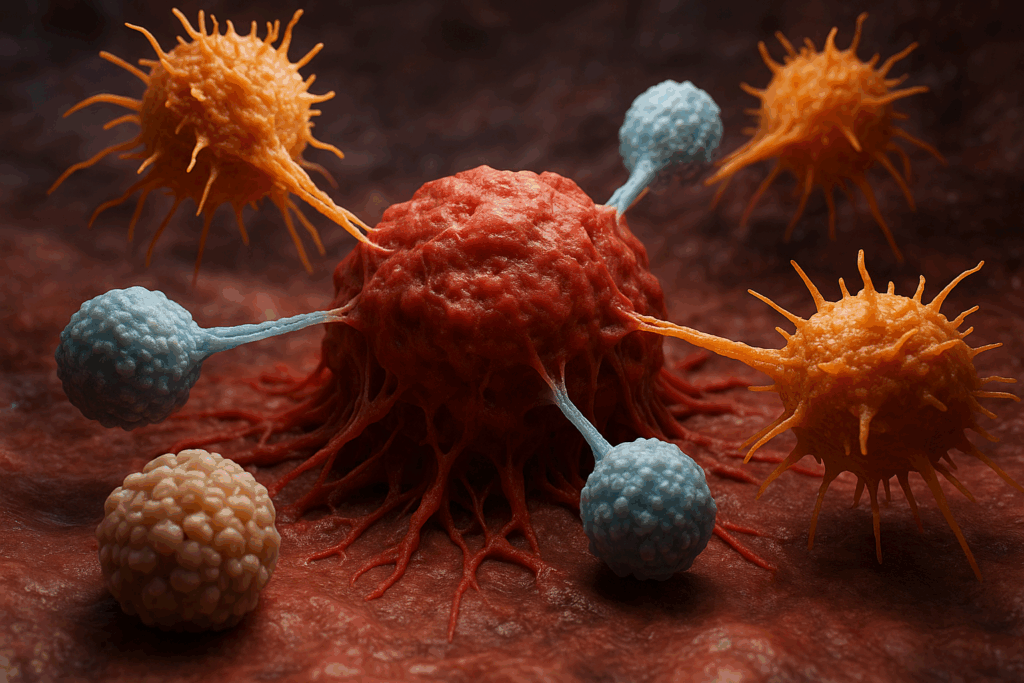
体の中で、それまで眠っていた免疫が、MHCの名札が見えた瞬間に目覚めて一斉に動き出す、まるで火災報知器が鳴って、消防士が一斉出動するような変化が、体の中で起きているのです。
この治療法は、2001年から2025年までに約1万6千人以上(※)の方に行われてきました。対象となったがんの種類も様々です。
(※上記人数・症例数は、当院グループおよび関連施設・関連研究において検査・治療プロセスに関与した累積件数の整理であり、治療効果(有効性)や生存率等を示すものではありません。集計期間:1997年10月24日〜2023年10月31日
これまで治療対象となった主ながん種別と症例数
| 胃がん | 1,221人 | 切除できない進行例が多い |
| 肺がん | 1,480人 | 非小細胞肺がんが中心 |
| 乳がん | 1,778人 | 再発やホルモン不応例が多い |
| 膵臓がん | 1,100人 | 多くが切除不能例 |
| 大腸がん | 1,474人 | 転移例が多い |
| 前立腺がん | 731人 | 再発・転移がんが多い |
| その他のがん | 8,155人 | 食道・胆道・卵巣など、さまざまな臓器 |
※症例の病期・治療内容・併用治療・評価方法は症例ごとに異なります。適応可否は検査結果・病状等を踏まえ医師が個別に判断します。
無料アドバイス LINEで写真を送るだけ
実際の治療と補助療法
MHCクラスI誘導型がん免疫治療は、単なる1回の処置ではなく、段階的なプロセスによってがん免疫の再起動を目指しています。
免疫状態の把握(Risk Checker検査)
高度精密血液検査リスクチェッカー採血によって、IL-6、IFN-γ、腫瘍マーカー、T細胞のバランス(Th1/Th2)などを測定。AI解析により、がんの進行度と免疫環境の状態をスコア化。
MHCクラスI誘導のための点滴治療
がん細胞にMHCクラスI複合体の再発現を促す主軸治療。臨床実績に基づいた複数の製剤から、患者ごとに最適な処方を選択。
補助療法の併用
患者の状態に応じて、以下のような補助製剤を組み合わせて使用。
経過の追跡と調整
定期的な免疫・腫瘍マーカーの再検査。治療効果の可視化と、次の投与設計へのフィードバック。必要に応じて標準治療との併用や個別調整も実施。
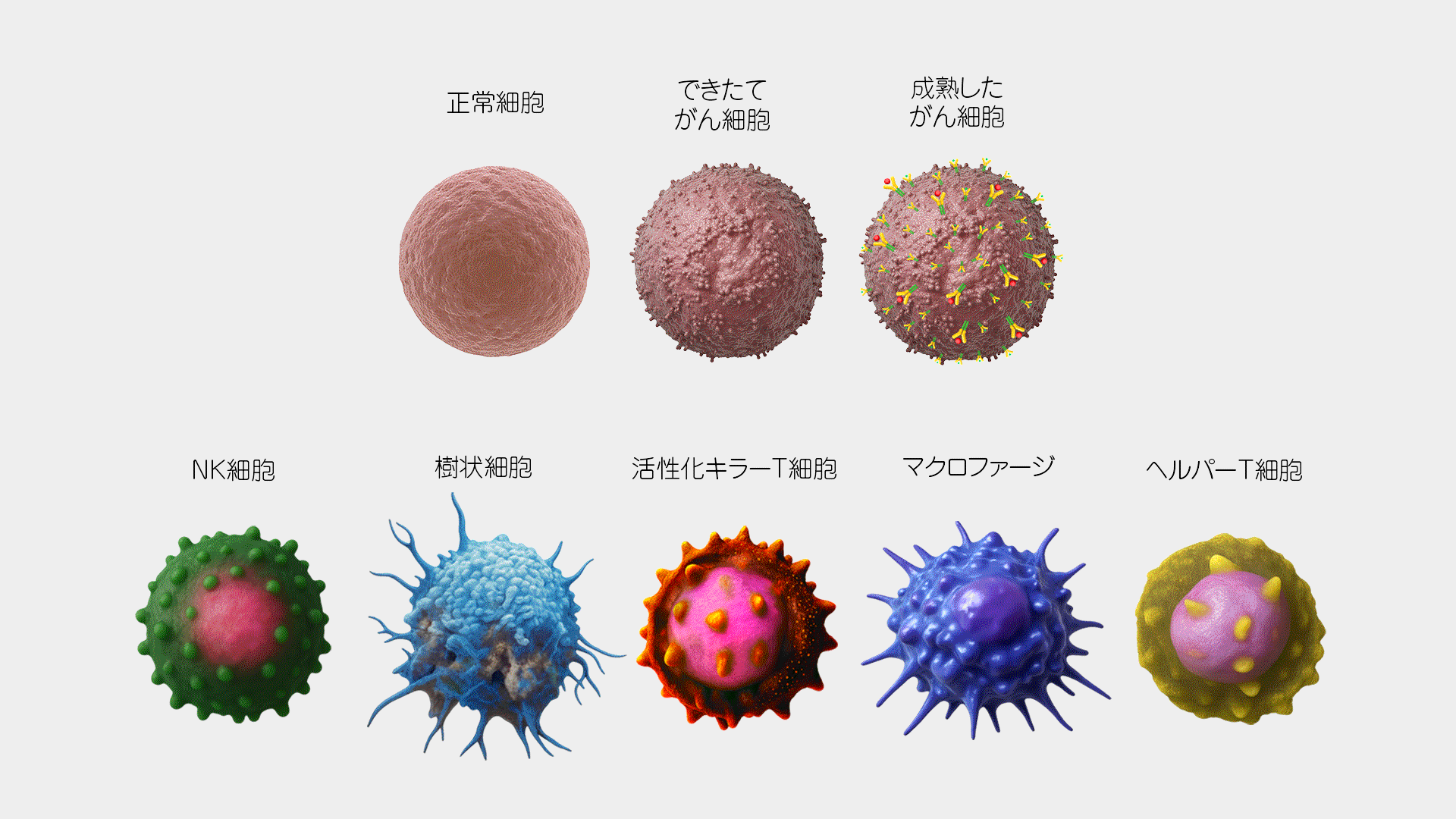
免疫細胞は、がん細胞だけが放出する「がんペプチド」という特殊な物質(タンパク質)を目印に、がんへの攻撃を仕掛けるとお伝えしてきました。しかし増殖を繰り返すがん細胞には、この「がんペプチド」を細胞内に隠し、免疫細胞からの攻撃を避ける術を備えています。そのため当院ではまず最初に「がんの目印」を出現させ、免疫細胞を誘導・誘発させることを目的に治療を開始いたします。
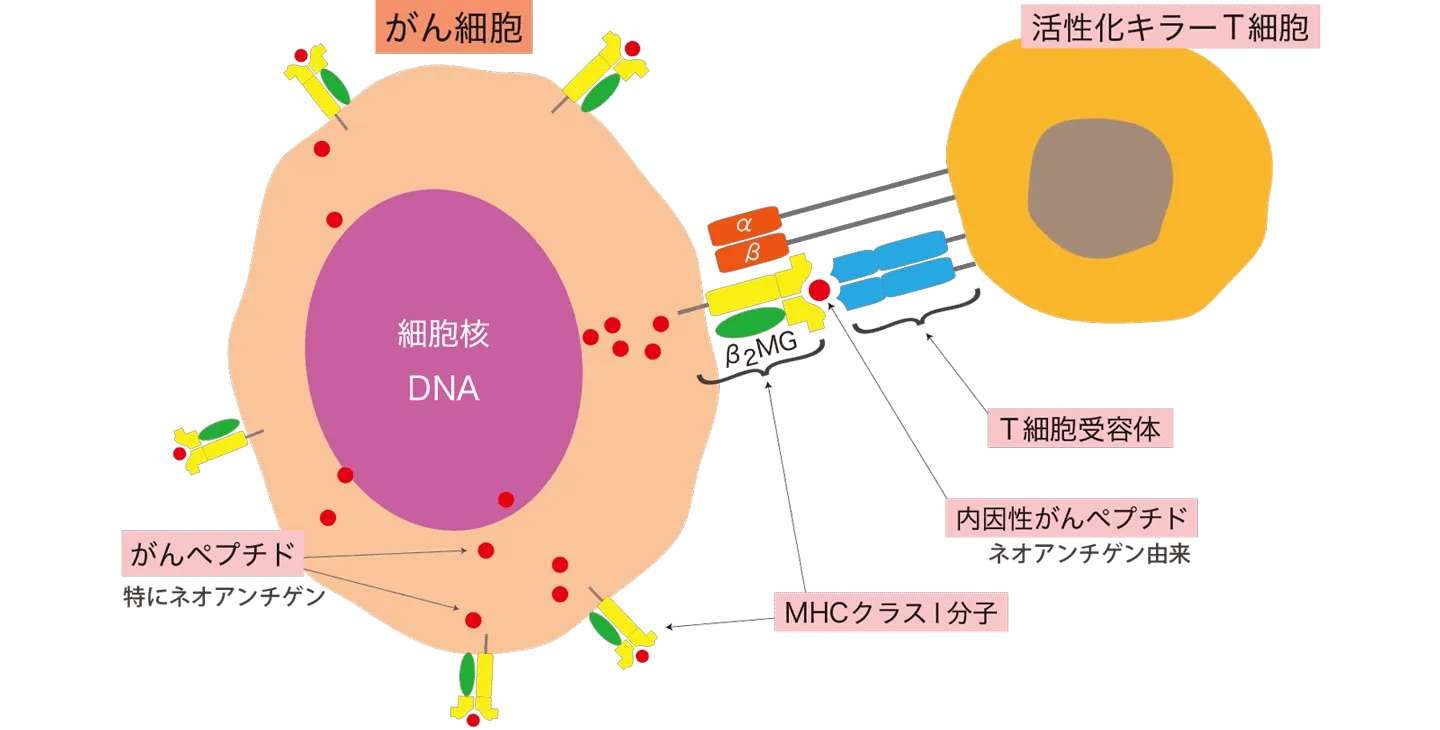
内因性ペプチド誘導
隠れたMHCクラスI分子を引っ張り出し、免疫機能にがんの目印を教え続ける
転移を繰り返す進行性のがん細胞は、活性化キラーT細胞からの攻撃を逃れるため、自分自身の目印MHCクラスI分子をがん細胞の中に隠してしまう場合があります。その隠れたMHCクラスI分子を引っ張り出し、免疫機能にがんの目印を教え続けることを目指したものが、内因性ペプチド誘導です。
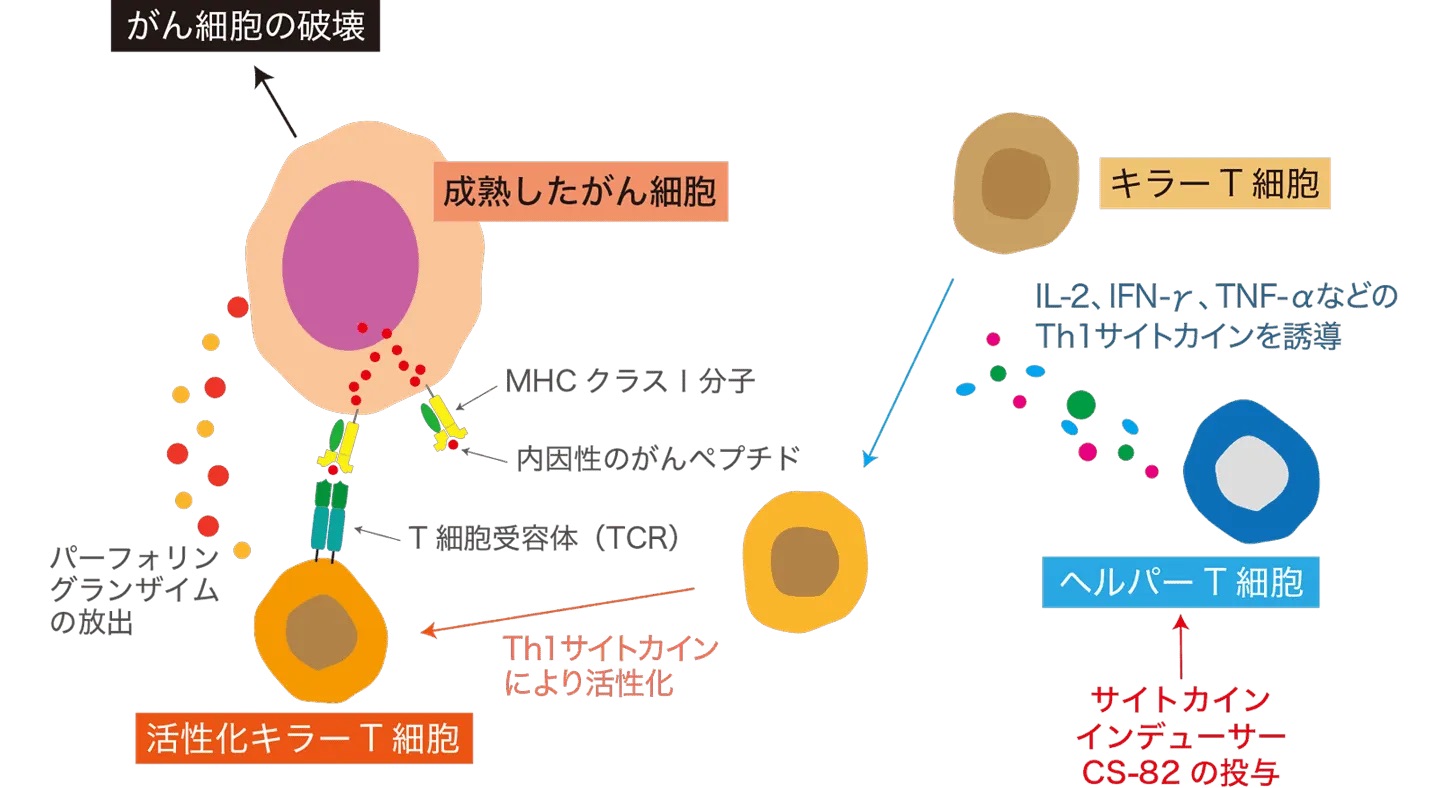
サイトカイン誘導
発現させた内因性ペプチドを目印に活性化キラーT細胞にがん細胞を強力に攻撃させる
免疫機構をかいくぐったがん細胞が体内に定着すると、初めのうちはがん細胞と免疫細胞ともに互角に闘う環境が作られますが、やがてがん細胞の活発化によって免疫力に弱体化が生じると、免疫疲弊(めんえきひへい)という状況に陥る場合があります。「サイトカイン」の生産を促し、がん細胞への攻撃力を回復させることを目指した治療手段です。

アポトーシス誘導
がん細胞が無限に増殖しつづける原因(がん細胞がミトコンドリアに甚大な障害を与えている)を改善
正常な細胞は細胞に異変が生じた際、ミトコンドリアによって自ら自滅を行おうとする反応「アポトーシス(プログラムされた細胞死)」が発令されます。がん細胞が無限に増殖しつづける理由には、がん細胞がミトコンドリアに甚大な障害を与えている可能性があるためであり、この改善が急がれます。
※免疫抑制物質を排除する際に、稀に副作用として顔のほてりなどが生じる可能性があります。
免疫治療と併用
上記で述べた免疫治療手法は、ネオアンチゲン複合免疫治療の根幹をなすものでした。しかし、遺伝子/DNAの突然変異によって生じるがん腫瘍の原因はさまざまです。そこで、難治性の進行がんに伴いやすい以下の病態にもそれぞれの治療手法が用意されています。
悪液質の対策
グレリン様物質製剤の応用
がん細胞の増大にともなう病状の一つに、免疫細胞の著しい消耗や活性化因子(サイトカイン)の無秩序な暴走によって急速に病状を悪化させてしまう「悪液質」があります。リスクチェッカー検査によってこうした病状の併発を認めた場合には、即座にグレリン様アミノ酸ペプチド製剤の投与を実施します。
この製剤の特徴は、体内でのタンパク質の合成促進による「MHCクラスⅠペプチド」発現に寄与し、進行がんのような急な治療対処を要する病状に有益な点と考えられています。こうした治療手法はNEO AGING(ネオエイジング)という細胞老化制御理論より新たに導き出された治療手法の一つであり、今後の更なる治療応用を進めています。
サイトカイン・ストーム対策
ヒストン脱アセチル化の応用
同じく高度の進行がんにおいて、時に「炎症性サイトカイン」という活性化因子の無秩序かつ急速な増加が認められる場合があります。こうした原因には長期間にわたって継続した免疫疲弊の最終形態や、がんに関連した遺伝子の突然変異が原因であることが判明しつつあります。
そこで、このような病態に陥って炎症性サイトカインの暴走が生じた際には、ヒストン脱アセチル化対策を併用します。この治療手法は、活動を開始した変異遺伝子/DNAの活動を抑止する「遺伝子サイレンシング」効果を目的としたものであり、NAD+(ナッド)と呼ばれる補酵素の誘導体を経口投与することで容易に実施が可能です。
もちろん、前述した免疫治療と同様、当院においてこれまで副作用/副反応の出現した例は一例もなく、安全性に優れた治療手段であると認識しています。(2020年よりの投与症例による)
MHCクラスI複合型免疫治療の
メリット
一般的に副作用が少ないとされる免疫療法
免疫のはたらきを利用する治療のため、治療の影響のあらわれ方が、他の治療と異なる場合があります。しかしながら、選択した治療手法によっては事前に注意も必要な治療があることも忘れてはなりません。あらかじめ担当医にご確認ください。
利用可能ながんが広範囲にわたる
免疫治療は免疫応答の活性化というメカニズムにより、その効果は全身に及びます。そのため、再発・転移性がんのほか、高度進行がんや末期がんでさえ治療応用が可能となります。
標準治療との併用
近年では「免疫化学療法」という概念により、従来の抗がん剤との併用もしばしば行われるようになりました。もちろん、手術や放射線治療との併用も可能です。
一人一人に合わせた治療が可能
各症例に応じた病状や、免疫治療エビデンスとしてのがん専門/免疫複合検査プログラム(リスクチェッカー検査)などの結果を踏まえ、各種の治療カスタマイズが可能です。
MHCクラスI複合型免疫治療の
デメリット(副作用)
| MHCクラスⅠペプチド誘導 | 使用する注射製剤を点滴投与する際、稀に顔のほてり感を自覚する場合があります。(発現エビデンス:1%以下) |
| なお、採血/点滴時に消毒用アルコール綿を使用した場合、稀に皮膚の軽い赤みを生じる場合があります。(発現エビデンス:5%程度) | |
| アポトーシス誘導 | 粉末に調剤された内服剤を空腹時に内服した場合、稀に胃部に清涼感を感じる場合があります。(発現エビデンス:3%以下) |
| サイトカイン誘導 | カプセル形状の本製剤を服用開始した初期に1~2日ほど便秘生じた例があります(発現エビデンス:1%以下) |
| 遺伝子サイレンシング(ヒストン脱アセチル化誘導) | カプセル形状の製剤を服用開始後、初日に便秘傾向を示した例があります(発現エビデンス:3%以下) |
| 悪液質対策(グレリン様アミノ酸ペプチド製剤) | 口腔内崩壊錠という性質により、服用後に口腔粘膜の荒れが認められたケースがあります。(発現エビデンス:5%前後) |
無料アドバイス LINEで写真を送るだけ


